Weltweit werden jährlich etwa 15 Millionen Babys zu früh geboren, und diese Zahl ist weiter steigend. Industrienationen sind von dieser Entwicklung nicht ausgenommen. In Deutschland liegt die Rate laut der Weltgesundheitsorganisation WHO bei 9,2 pro 100 Neugeborene. Eine der am häufigsten auftretenden Komplikationen bei Frühchen ist die Bronchopulmonale Dysplasie, eine chronische Lungenerkrankung, die durch die oftmals notwendige künstliche Beatmung ausgelöst wird. Auch das Immunsystem der Frühchen ist nicht ausgereift, daher haben sie zudem ein erhöhtes Infektionsrisiko.
Lungeninfektionen werden am besten mit Medikamenten zum Inhalieren behandelt. Speziell an die Bedürfnisse von Neu- und Frühgeborenen angepasste Inhalationssysteme sind jedoch nicht verfügbar. Entsprechende Technologien sind aufgrund der spezifischen Atemeigenschaften der Winzlinge sehr anspruchsvoll:
- Charakteristische Merkmale der kleinen Patienten sind eine hohe Atemfrequenz von 40 bis über 60 Atemstöße pro Minute.
- Kurze Inhalationsperioden von 0,25 bis 0,4 Sekunden.
- Die neonatale Lunge weist nur kleine Atemzugvolumen auf.
Diese Faktoren erschweren die inhalative Behandlung zusätzlich. Daher entwickeln Wissenschaftlerinnen und Wissenschaftler des Fraunhofer-Instituts für Toxikologie und Experimentelle Medizin ITEM in Hannover gemeinsam mit Partnern aus Industrie und Forschung ein neues Inhalationssystem, das eine effiziente und schonende inhalative Therapie von Frühgeborenen ermöglicht.
Herausforderungen der inhalativen Medikamentengabe bei Frühgeborenen
»Die inhalative Medikamentengabe bei Frühchen ist schwierig. Die derzeitige kontinuierliche Zufuhr der Aerosole, also der Arzneimittel in Partikelform, in den Atemstrom ist nicht effizient. Zum einen geht ein Großteil des teuren Medikaments aufgrund des Inhalations-Exhalationsverhältnisses verloren und weist somit keinen medizinischen Nutzen auf. Zum anderen wird das Aerosol durch den Atemstrom, der durch das Beatmungsgerät fließt, sofort verdünnt«, sagt Dr. Gerhard Pohlmann, Leiter des Bereichs »Translationale Medizintechnik« am Fraunhofer ITEM.
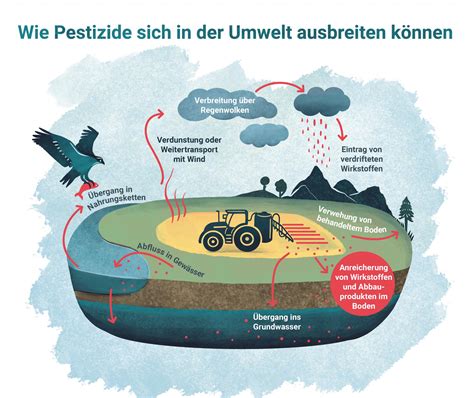
Innovatives atemgetriggertes Inhalationssystem
Die Projektpartner setzen mit ihrer neuen Entwicklung auf eine atemgetriggerte Zugabe direkt am Patienten. Dabei wird das Aerosol dem Frühchen direkt an der Nase und ausschließlich beim Einatmen verabreicht.
»Somit ist erstmals eine hocheffiziente Medikamentengabe für Frühgeborene realisierbar. Die Wirkstoffmenge lässt sich reduzieren, die Therapiedauer verkürzen. Eine genaue Zeitsteuerung mit sehr kurzen Inhalationsboli erlaubt zudem die fokussierte Behandlung bestimmter Lungenregionen«, so Pohlmann.
Ein vergleichbares System eignet sich grundsätzlich auch für erwachsene Patienten, die täglich inhalativ therapiert werden müssen. Eine Verkürzung der Anwendungszeit kann deren Lebensqualität entscheidend verbessern.
Technologie des neuartigen Inhalationssystems
Das neuartige Inhalationssystem kombiniert zwei Technologien:
- Nasenstecker (nasaler Prong) mit Miniaturaerosolventil: Dieser wird direkt an der Nase des Frühchens angebracht. Das Aerosolventil mit einer Reaktionszeit im Bereich von wenigen Millisekunden erlaubt die schnelle und gezielte Freisetzung des Wirkstoffs.
- Sensorfolie: Der Nasenstecker ist mit einer Sensorfolie gekoppelt. Auf die Bauchdecke des Frühchens aufgelegt, erfasst diese flexible Matrix mit Dehnungssensoren die Kontraktionen des Oberbauchs und misst so den exakten Zeitpunkt, an dem das Baby einatmet.
Für die präzise Aerosolfreigabe steuert das Messsignal das Mikroventil über einen intelligenten Algorithmus an. »Der Zeitpunkt des Einatmens muss mit einer Genauigkeit von etwa 20 Millisekunden getroffen werden. Das Platzieren normaler Sensoren im Ausatembereich eines Beatmungsgerätes erlaubt eine derart genaue Erfassung nicht«, erläutert der Forscher.
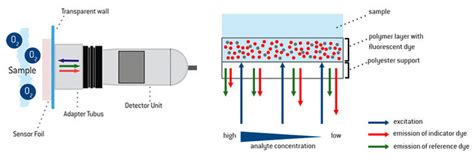
Vorteile der ventilator-unabhängigen Atemerfassung
Derzeit verfügbare Systeme zur Atemtriggerung von Inhalationssystemen sind entweder auf die Messung des Atemsignals im Beatmungsschlauch angewiesen oder über eine elektrische Verbindung an das Ventilationssystem gekoppelt. »Unsere ventilator-unabhängige Atemerfassung erspart den Eingriff in ein bereits zugelassenes Gerät und senkt damit Zulassungshürden.«
Die Sensorfolie mit ultradünnen Chips und die Entwicklung der Atemtriggerung wird im Projekt »FLEXMAX« in einem Konsortium realisiert. Das Bundesministerium für Bildung und Forschung BMBF fördert das Vorhaben, das zentrale Punkte der Ausschreibung »Neue Elektroniksysteme für intelligente Medizintechnik (Smart Health)« adressiert.
Ergebnisse und Ausblick
In Tests mit Erwachsenen sowie in Versuchen mit Geräten, die die Atmung von Frühgeborenen simulieren, konnte eine Effizienzsteigerung von 60 Prozent gegenüber herkömmlicher Inhalationstechnologie erreicht werden.
Um die Sensorfolie in einer frühen Phase praxisnah testen zu können, entwickeln die Projektpartner zudem eine künstliche Bauchdecke, die sich wie die eines Frühgeborenen bewegt.
Das komplette Inhalationssystem liegt derzeit als Demonstrator vor. Bis zur Serienreife seien noch etwa drei bis fünf Jahre einzuplanen, so Pohlmann.
Weitere Forschungsansätze am Fraunhofer ITEM
Das Expertenteam des Fraunhofer ITEM forscht zudem an Applikationssystemen für die inhalative Verabreichung von Trockenpulverformulierungen, beispielsweise um Frühchen mit Atemnotsyndrom zu therapieren.
Das Syndrom tritt auf, wenn die nicht ausgereifte Lunge kein oder zu wenig Surfactant bildet. Ohne Surfactant, das die Oberflächenspannung in den Lungenbläschen herabsetzt, kann sich die Lunge nicht entfalten. Das Baby leidet an Sauerstoffmangel und Atemnot und muss künstlich beatmet werden.
Üblicherweise wird aus Tierlungen gewonnenes Surfactant als Suspension in die Lunge gespült. Das Problem: Diese sogenannte Instillation ist traumatisch und das als Suspension zugeführte Surfactant verteilt sich nicht so gleichmäßig im Atmungsorgan wie bei der Zuführung als Aerosol. Verabreicht man das Surfactant hingegen als befeuchtetes Trockenaerosol inhalativ, verteilt es sich homogener und wirkt besser.
Wärmemanagement bei Frühgeborenen
Seit der Zeit, als Frühchen von Dr. Martin Couneys Krankenschwestern auf Coney Island, New York, USA, in winzigen Glasschränken versorgt wurden, hat sich die medizinische Versorgung von Neugeborenen drastisch geändert. Im Lauf der Jahre wurden viele einfache und andere neuartige Techniken und Therapien eingeführt und umgesetzt, da heute bereits sehr unreife und fragile Kinder entbunden werden können. Die immer komplexer werdende Situation extrem frühgeborener Säuglinge bringt ganz eigene Herausforderungen mit sich, nicht zuletzt die Schwierigkeit, die Kinder warm zu halten. Wärmeregulierung und Verhinderung einer Unterkühlung stehen bereits ganz oben auf der Prioritätenliste, wenn Entbindungsstationen gesunde, reif geborene Kinder zur Welt bringen. Bei noch deutlich fragileren Kindern mit sehr niedrigem Geburtsgewicht (VLBW) sind aber möglicherweise andere Techniken notwendig, um einen gefährlichen Abfall der Körperkerntemperatur zu verhindern.
Internationale Empfehlungen verlangen, dass die Körperkerntemperatur eines Neugeborenen in einem Bereich von 36,5 °C - 37,5 °C gehalten wird, um die besten Ergebnisse für das Baby zu erzielen [1].
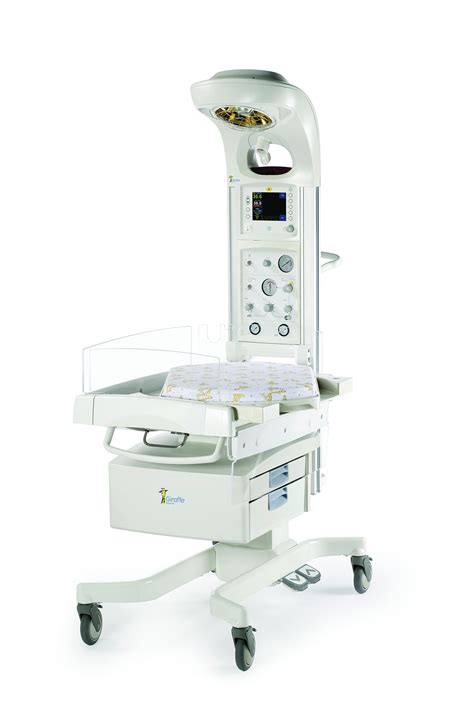
Es gibt verschiedene Geräte, die in Situationen, in denen Säuglinge schnell auskühlen, nützlich sind [2]. In diesem Blog geht es speziell um die Zuführung erwärmter Gase bei der respiratorischen Unterstützung von VLBW-Kindern, die bei vielen Frühgeburten notwendig ist.
Klinische Studien, insbesondere die Studie von Meyer et al aus dem Jahr 2014 [5], haben die Vorteile der Verwendung erwärmter Gase bei der Stabilisierung von VLBW-Säuglingen und der Überdruckbeatmung (PPV) gezeigt. Das Konzept ist nicht fremd; schließlich ist es allgemein anerkannt und gängige Praxis, dass alle therapeutischen und unterstützenden akuten Atemwegstherapien auf der Neugeborenenstation mit aktiver Wärme und Befeuchtung durchgeführt werden.
Die derzeitige Praxis in vielen Ländern sieht vor, dass für die Atemunterstützung von Neugeborenen ein Plattformbett (z. B. Bild 2 oben) und eine Reanimationsvorrichtung mit T-Stück, das in das aufrechte Stativ am hinteren Ende des Bettes eingebaut ist, verwendet wird. Dadurch kann bei den 10 % der Kinder, die bei ihrer Geburt nicht atmen, die erforderliche Unterstützung nahezu sofort eingeleitet werden [6]. Allerdings stammen die über dieses PPV-System abgegebenen Gase direkt aus einem Gasanschluss oder aus Gasflaschen und sind daher „kalt und trocken“. Tatsächlich ergab eine in verschiedenen Bereichen eines Krankenhauses durchgeführte Untersuchung, dass zugeführter Sauerstoff eine mittlere Temperatur von 23,3 °C und eine relative Luftfeuchtigkeit (RH) von nur 2,1 % aufwies, während in der Leitungsluft eine Temperatur von 23,4 °C und eine RH von 5,4 % gemessen wurde [7].
Wenn ohnehin fragile VLBW-Säuglinge eine PPV erhalten und mit diesen kalten und trockenen Gasen stabilisiert werden, liegt es nahe, davon auszugehen, dass die Körpertemperatur der Kinder dadurch über den empfohlenen Bereich hinaus absinken könnte. Auf jeden Fall aber tragen die kalten und trockenen Gase angesichts der massiven Auswirkungen von Leitung, Konvektion, Strahlung und Verdunstung [8] auf diese Frühgeborenen nicht dazu bei, dem mit diesen thermodynamischen Kräften und deren Nutzung verbundenen Wärmeverlust entgegenzuwirken, wie es durch die Anwendung erwärmter und befeuchteter Gase möglich wäre.
Ein weiterer wichtiger Punkt, der für die Verwendung erwärmter und befeuchteter Gase spricht, sind ihre positiven Auswirkungen auf die Verbesserung der Lungenfunktion. Das PPV-System lässt sich leicht in eine beheizte, befeuchtete Version umwandeln, indem man einen alternativen Schlauchsystem-Typ anstelle des einfachen Schlauchschenkels und ein Winkelstück zur Druckanpassung wählt, die mit Standard-Schlauchsystemoptionen geliefert werden. Ein beheiztes, befeuchtetes T-Stück-Schlauchsystem umfasst einen beheizten Schenkel und eine Befeuchtungskammer, die beide in Verbindung mit einem elektrischen beheizbaren Atemluftbefeuchter arbeiten, um dem System Wärme und Wasserdampf zuzuführen, während Gas durch die Befeuchtungskammer strömt. Diese Art von System ist auf Neugeborenen-Intensivstationen weltweit häufig im Einsatz und kann daher den Bedarf an zusätzlicher Einarbeitung verringern. In Anbetracht der Tatsache, dass eine derart einfach zu implementierende Lösung ohne Weiteres verfügbar ist, wäre die Änderung der Praxis und der Richtlinien sowie die zu leistende Überzeugungsarbeit unter Umständen weniger aufwändig als erwartet.
Da bei Frühgeborenen unabhängig vom Setting immer ein sehr reales Risiko einer Unterkühlung besteht, ist es als Vorteil zu betrachten, dass uns so viele Möglichkeiten zur Verfügung stehen, um ein positives Ergebnis zu erzielen. Während die Implementierung bereits einer solch einfachen Veränderung der gängigen Praxis die Temperatur bei der Aufnahme auf die Neugeborenenstation verbessern könnte, könnte es einen lohnenden Effekt auf die Körpertemperatur dieser empfindlichen Kinder haben, alle Optionen und die Möglichkeit der Durchführung mehrerer vorteilhafter Interventionen auszuloten.
Die Umstellung auf das selbständige Atmen bei einem Neugeborenen ist die komplexeste physiologische Anpassung, die der Mensch zu leisten hat [10], und allzu oft benötigen Neugeborene dabei Unterstützung. Aber auch durch eine thermoneutrale Umgebung sind sie zunächst noch nicht für eine „aktive“ Wärmeproduktion konzipiert. sind dazu besser in der Lage.
Ursachen für Wärmeverluste bei Frühgeborenen
Der Fetus produziert durch einen höheren Metabolismus Wärme und hat intrauterin eine um ca. 1 °C höhere Körpertemperatur als die Mutter [5]. Die Plazenta fungiert dabei als Wärmetauscher. Bei der Geburt wird das Neugeborene aus der warmen, feuchten Umgebung der Gebärmutter in eine ungeschützte Umgebung mit einer Temperatur von etwa 25 °C ersetzt [6]. Dies führt zu einem schnellen Wärmeverlust.
Die wichtigste Ursache für Wärmeverluste bei Frühgeborenen ist die Perspiratio insensibilis, der unmerkliche Wasserverlust über die Haut. Die unreife Hautbarriere von Frühgeborenen ist durchlässiger, was zu einem erhöhten Wasser- und Wärmeverlust führt.
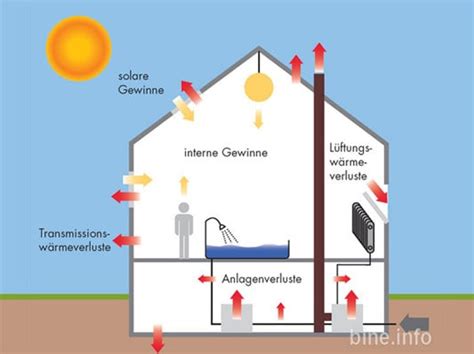
Weitere Faktoren, die zu Wärmeverlusten beitragen:
- Konvektion: Wärmeabgabe an die umgebende kalte Luft.
- Konduktion: Direkter Wärmeübergang an kältere Oberflächen (z. B. Liegefläche).
- Strahlung: Wärmeabgabe an kühlere Objekte in der Umgebung.
- Verdunstung: Wärmeentzug durch Verdunstung von Feuchtigkeit auf der Haut.
Die Körperoberfläche im Verhältnis zur Körpermasse ist bei Frühgeborenen sehr groß, was die Wärmeabgabe weiter erhöht.
Temperaturmanagement und Monitoring
Die Aufnahmetemperatur auf der Intensivstation nach Erstversorgung im Kreißsaal ist ein bedeutender Qualitätsindikator für das neonatologische Management. Eine Hypothermie bei der Aufnahme ist mit einer erhöhten Mortalität verbunden.
Die rektale Messung der Körperkerntemperatur gilt als die klassische Methode. Zentrale Messstellen liegen abdominal über der Leberregion und dorsal interskapulär. Periphere Temperaturmessung erfolgt an der Hand oder dem Fuß.
Die Zwei-Punkt-Temperaturmessung wird zum Infektionsmonitoring und der Detektion von Auskühlung bei Pflegemaßnahmen eingesetzt.
Wärmemanagement im Kreißsaal
Ein effektives Wärmemanagement im Kreißsaal umfasst:
- Vorgewärmte Tücher und Windeln.
- Die Verwendung von Wärmeschränken.
- Die Nutzung von beheizbaren Babywiegen oder Wärmelampen.
- Das sofortige Abtrocknen des Neugeborenen nach der Geburt.
- Bei Frühgeborenen unter 29 SSW die Verwendung von Plastikkappen.
Hautbarriere und ihre Bedeutung
Die Haut von Frühgeborenen ist strukturell noch unreif. Sie ist dünner, die elastischen Fasern und die ekkrinen Schweißdrüsen sind unreif, was zu einer unreifen Hautbarriere führt. Dies bedingt eine erhöhte Anfälligkeit für Infektionen und eine erhöhte Verletzlichkeit durch mechanische Traumata. Zudem ist die Hautbarriere weniger effektiv im Schutz vor Wasserverlust und der Regulierung der Körpertemperatur.
Die Messung des transepidermalen Wasserverlustes (TEWL) und des Hautoberflächen-pHs gibt Aufschluss über den Zustand der Hautbarriere. Bei Frühgeborenen zeigen sich im Verlauf der ersten Lebenswochen Veränderungen dieser Parameter, was die Notwendigkeit einer angepassten Hautpflege unterstreicht.
Die Messungen wurden bis zum 7. Tag und in der Folge bis zur 7. Lebenswoche durchgeführt. Die Hautoberflächen-pH-Werte waren bei Kindern mit Gestationsalter zwischen 30 und 37 vollendeten Schwangerschaftswochen, die vaginal entbunden wurden, signifikant niedriger als bei Kindern, die per Kaiserschnitt entbunden wurden.
Es ist wichtig, die Hautbarriere zu schützen, um Wärmeverluste und Infektionen zu minimieren.
Routinepflege und Beobachtung des Neugeborenen
Während des Krankenhausaufenthalts lernen frischgebackene Eltern, wie sie ihr Neugeborenes füttern, baden und anziehen. Vor der Entlassung besprechen Ärzte mit den Eltern die Routineaspekte der Pflege in Bezug auf Nabelschnur, Beschneidung, Gewicht sowie Urin- und Stuhlgang.
Nabelschnurpflege
Die Nabelschnurklemme kann entfernt werden, wenn die Nabelschnur trocken erscheint, meist nach etwa 24 Stunden. Die Nabelschnurpflege zielt darauf ab, das Risiko einer Nabelschnurinfektion (Omphalitis) zu reduzieren. Der Nabelschnurrest sollte trocken und sauber gehalten werden. Eine trockene Schnurpflege oder -reinigung mit Seife und Wasser ist meist ausreichend; topische Mittel verringern das Infektionsrisiko nicht.
Gewicht und Ausscheidungen
Die meisten Neugeborenen verlieren in den ersten Lebenstagen 5-7% ihres Geburtsgewichts, primär bedingt durch Urin und Perspiratio insensibilis. Der Urin kann die Windel in den ersten Lebenstagen durch Uratkristalle orange oder rosa verfärben. Die meisten Neugeborenen scheiden den ersten Urin innerhalb von 24 Stunden postnatal aus.
Wenn innerhalb der ersten 24 Stunden kein Mekonium abgesetzt wird, sollte eine Abklärung nach weiteren Fehlbildungen erwogen werden.
Krankenhausentlassung
Neugeborene, die innerhalb der ersten 48 Stunden entlassen werden, sollten nach 2-3 Tagen einen Kontrolltermin haben, um das Trinkverhalten, das Gedeihen, die Hydratation und den Grad der Gelbsucht zu beurteilen.
tags: #perspiratio #insensibilis #fruhgeborene