Die Immuntherapie hat die onkologische Behandlungslandschaft revolutioniert und stellt einen der bedeutendsten Fortschritte der modernen Onkologie dar. Lange Zeit galt das Mammakarzinom als Tumor mit geringer Immunogenität, was als „kalter“ Tumor bezeichnet wurde. Neue Erkenntnisse über die immunologische Beteiligung, insbesondere die prognostische Bedeutung von tumorinfiltrierenden Lymphozyten (TILs) bei triple-negativem und HER2-positivem Brustkrebs, haben diese Annahme jedoch in Frage gestellt. Diese Entwicklungen deuteten darauf hin, dass eine Verstärkung der antitumoralen Immunität klinisch relevant sein könnte, was die Grundlage für die Entwicklung der Immuncheckpoint-Inhibition (ICI) beim Mammakarzinom schuf.
Fortschritte der Immuncheckpoint-Inhibition beim Mammakarzinom
Das schwer zu behandelnde triple-negative Mammakarzinom (TNBC) profitiert zunehmend von der Immuntherapie. Die amerikanische Arzneimittelbehörde FDA erteilte bereits die erste Zulassung für einen PD-L1-Inhibitor (Atezolizumab) in Kombination mit Chemotherapie zur Behandlung des TNBC. Es wurde jedoch festgestellt, dass die Immuntherapie bei PD-L1-Immunzell-negativen Tumoren keine Aktivität zeigt. Aktuelle Daten der Studie KEYNOTE-086 zum PD-L1-Inhibitor Pembrolizumab lieferten vielversprechende Ergebnisse.
Insgesamt erreichten 7,6 % der Patientinnen ein Ansprechen auf die Therapie. Davon sprachen 9,5 % der Patientinnen mit PD-L1-positivem und 4,7 % mit PD-L1-negativem Tumorstatus an. In der Kohorte B, die 84 Patientinnen mit positivem PD-L1-Tumorstatus (tumor PD-L1 combined positive score, CPS ≥ 1) in der Erstlinie einschloss, war die Gesamtansprechrate mit 23,1 % noch höher als in späteren Therapielinien.
Checkpoint-Inhibitoren bei frühen und fortgeschrittenen gynäkologischen Karzinomen
Checkpoint-Inhibitoren wie der PD-1-Inhibitor Pembrolizumab haben sich auch bei frühen und fortgeschrittenen triple-negativen Mammakarzinomen (TNBC) sowie fortgeschrittenen Endometrium- und Zervixkarzinomen etabliert. Expert:innen diskutierten auf einem Symposium im Rahmen des Deutschen Krebskongresses (DKK) 2022 den aktuellen Zulassungsstatus und Studiendaten.
Triple-negatives Mammakarzinom (TNBC)
Angesichts der ungünstigen Prognose bei TNBC besteht ein hoher Bedarf an neuen Therapieoptionen. Studien wie IMpassion031 mit Atezolizumab und KEYNOTE-522 mit Pembrolizumab haben in Kombination mit Chemotherapie (Chemo) in der Neoadjuvanz zu einer verbesserten pathologischen Komplettremission (pCR) beigetragen, die mit einer günstigeren Prognose assoziiert ist.
In der Studie KEYNOTE-522 verbesserte die neoadjuvante Behandlung mit Pembrolizumab plus Chemotherapie, gefolgt von adjuvanter Pembrolizumab-Monotherapie, im Vergleich zur neoadjuvanten Chemotherapie und anschließender Placebo-Gabe bei Hochrisikopatientinnen den primären Endpunkt pCR (64,8 % vs. 51,2 %; p = 0,00055) unabhängig vom PD-L1-Status. Zudem wurde eine signifikante Verbesserung des ereignisfreien Überlebens (EFS) dokumentiert (36-Monats-EFS 84,5 % vs. 76,8 %; HR 0,63; p = 0,00031).
Auf Basis dieser Daten erhielt Pembrolizumab die EU-Zulassung für die neoadjuvante Therapie bei lokal fortgeschrittenen oder frühen TNBC mit hohem Rezidivrisiko. Seit November 2021 ist der PD-1-Inhibitor zusammen mit Chemotherapie auch bei lokal rezidiviertem, nicht resezierbarem oder metastasiertem TNBC mit einem PD-L1-Combined Positive Score (CPS) ≥ 10 zugelassen, sofern zuvor keine Chemotherapie im metastasierten Setting verabreicht wurde.
Die Zulassungsstudie KEYNOTE-355 zeigte, dass Pembrolizumab in Kombination mit nab-Paclitaxel, Paclitaxel oder Gemcitabin/Carboplatin im Vergleich zur alleinigen Chemotherapie das progressionsfreie Überleben (PFS) (median 9,7 vs. 5,6 Monate; HR 0,65; p = 0,0012) und das Gesamtüberleben (OS) (median 23,0 vs. 16,1 Monate; HR 0,73; p = 0,0093) signifikant verbesserte. Diese Ergebnisse sind klinisch hoch relevant.
Bei einem CPS ≥ 10 gilt Pembrolizumab/Chemotherapie als Erstlinienstandard bei einem therapiefreien Intervall (TFI) ≥ 6 Monate. Bei einem PD-L1 > 1 % in Immunzellen kann auch Atezolizumab plus nab-Paclitaxel eingesetzt werden, wenn das TFI mindestens 12 Monate beträgt.
Endometrium- und Zervixkarzinom
Auch bei Endometrium- und Zervixkarzinomen hat die Checkpoint-Inhibition an Bedeutung gewonnen. Die Kombination aus Pembrolizumab und dem Tyrosinkinase-Inhibitor Lenvatinib ist für das fortgeschrittene oder rezidivierte Endometriumkarzinom mit Progress während oder nach Platin-basierter Therapie zugelassen. In der KEYNOTE-775-Studie verbesserte diese Kombination signifikant das OS (HR 0,62; p < 0,0001) und PFS (HR 0,56; p < 0,0001) im Vergleich zu einer Monochemotherapie.
Ermutigende Überlebensdaten zeigte auch die KEYNOTE-158-Studie mit Pembrolizumab-Monotherapie bei dMMR/MSI-Tumoren. Das erreichte mediane OS von über 65 Monaten stellt einen „Quantensprung“ dar und dies bei einem gut handhabbaren Toxizitätsprofil. Basierend auf diesen Daten erhielt Pembrolizumab die Zulassung für dMMR/MSI-Tumoren; auch Dostarlimab-Monotherapie ist in diesem Setting zugelassen.
Seit Mai 2022 ist die Hinzunahme von Pembrolizumab zur Chemotherapie plus/minus Bevacizumab eine neue Standardtherapie für das rezidivierte/metastasiere Zervixkarzinom mit CPS ≥ 1.
Wie funktioniert die Immuntherapie? Kurzer Vergleich zur Chemotherapie.
Mechanismen der Checkpoint-Inhibition
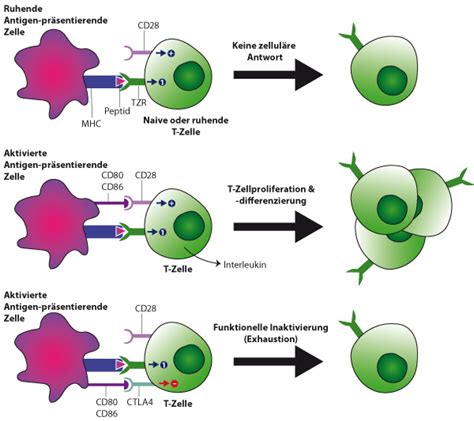
Checkpoint-Inhibitoren (auch Immuncheckpoint-Inhibitoren) sind Antikörper, die auf Oberflächenproteine wie CTLA-4 oder PD-1 bzw. dessen Liganden PD-L1 abzielen. Diese Proteine spielen eine Schlüsselrolle bei der Regulierung der Immunantwort, indem sie die Aktivität von T-Zellen steuern.
T-Zell-Rezeptoren und nachgeschaltete Signalkaskaden sind essenziell für die Auslösung von Effektorfunktionen des Immunsystems. Um eine überschießende Immunantwort zu verhindern, werden diese Signalkaskaden durch co-inhibitorische Oberflächenrezeptoren wie CTLA-4 und PD-1, die von T-Zellen exprimiert werden, reguliert.
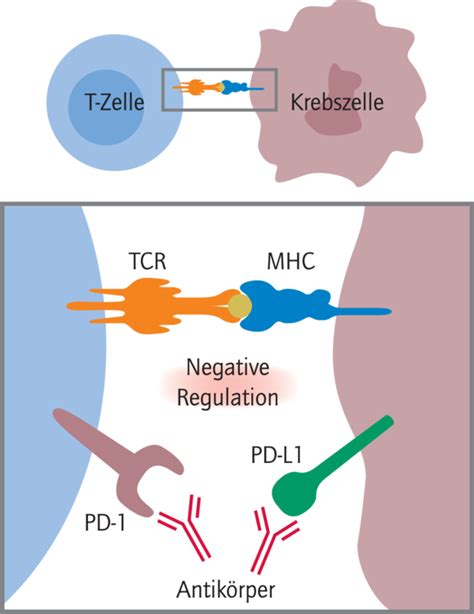
PD-1 und PD-L1
Tumorzellen können vermehrt co-inhibitorische Oberflächenproteine wie PD-L1 exprimieren, um Überwachungsmechanismen des Immunsystems zu umgehen. Die Bindung von PD-L1 an seinen Rezeptor PD-1 auf T-Zellen unterdrückt die immunologische Antwort. Durch die Blockade der Interaktion zwischen PD-1 und PD-L1 mittels Checkpoint-Inhibitoren wird diese T-Zell-Signalkaskade gehemmt, wodurch die T-Zell-Effektorfunktion gegenüber Tumorzellen wiederhergestellt werden kann.
CTLA-4
CTLA-4 wird von aktivierten T-Zellen induziert und wirkt hemmend auf deren Überaktivierung. Die therapeutische Blockade durch einen CTLA-4-Antikörper verhindert diese Inaktivierung, sodass die T-Zellen aktiviert bleiben und eine verstärkte Immunantwort, potenziell gegen den Tumor, auslösen können. CTLA-4-Inhibitoren können zudem die Funktion von antigenpräsentierenden Zellen (APC) wiederherstellen.
Klassifizierung und Anwendung von Checkpoint-Inhibitoren
Je nach targetiertem Oberflächenprotein lassen sich Checkpoint-Inhibitoren in folgende Untergruppen gliedern:
- Anti-CTLA-4-Antikörper (z.B. Ipilimumab, Tremelimumab): Hauptanwendung bei (metastasierenden) malignen Melanomen.
- Anti-PD-1-Antikörper (z.B. Nivolumab, Pembrolizumab): Zeigen gute Wirksamkeit bei Hodgkin Lymphom, aber auch Anwendung bei (metastasierenden) malignen Melanomen, nicht-kleinzelligem Lungenkarzinom (NSCLC), Nierenzellkarzinom (RCC), Kopf- und Halstumoren sowie bei urothelialen Karzinomen.
- Anti-PD-L1-Antikörper (z.B. Atezolizumab, Avelumab, Durvalumab): Anwendung bei (metastasierenden) malignen Melanomen, NSCLC, RCC, Kopf- und Halstumoren sowie bei urothelialen Karzinomen.
Studien zum Einsatz in weiteren Bereichen der Onkologie und Immunologie sind derzeit im Gange.
Nebenwirkungen und Management
Aufgrund ihrer immunstimulierenden Wirkung können Checkpoint-Inhibitoren zu überschießenden Reaktionen des Immunsystems führen. Dies kann die Induktion autoimmuner Reaktionen und die Verschlimmerung bestehender Autoimmunerkrankungen zur Folge haben.
Da Checkpoint-Inhibitoren als Antikörper keine Wechselwirkungen mit CYP-Enzymen eingehen, sind pharmakodynamische Wechselwirkungen unwahrscheinlich. Dennoch sollte die Anwendung systemischer Kortikosteroide vor Beginn einer Checkpoint-Inhibitor-Therapie vermieden werden, um eine verminderte Wirksamkeit zu verhindern.
Die gleichzeitige Einnahme einiger Checkpoint-Inhibitoren und Antikoagulanzien sollte engmaschig kontrolliert werden, um das erhöhte Risiko für gastrointestinale Blutungen zu minimieren. Aufgrund der Plazentagängigkeit von Checkpoint-Inhibitoren als humane IgG-Antikörper wird die Anwendung während der Schwangerschaft und bei Frauen im gebärfähigen Alter nicht empfohlen.
tags: #checkpoint #inhibitoren #gynakologie